アジスロマイシン分散錠
適応症
中耳炎、副鼻腔炎、咽頭炎、扁桃炎などの上気道感染症、気管支炎や肺炎などの下気道感染症。皮膚および軟部組織感染症、クラミジアトラコマチスによる単純性器感染症、非多剤耐性resistant菌による単純性器感染症(メルファラン種の組換え感染症)。
臨床薬理学
アジスロマイシンは、感受性の高い微生物の50代リボソームのサブユニットに結合することにより、タンパク質の合成を(核酸の合成に影響を与えることなく)阻害する作用機構を持つアザライド系抗生物質です。アジスロマイシンには、さまざまな病原性細菌に対する抗菌効果があります。グラム陽性好気性微生物:黄色ブドウ球菌、化膿連鎖球菌、肺炎連鎖球菌、溶血性連鎖球菌。アジスロマイシンは、エリスロマイシン耐性グラム陽性菌に対して交差耐性です。大部分のレンサ球菌(腸球菌)およびメチシリン耐性ブドウ球菌は、この製品に対して耐性があります。グラム陰性好気性微生物:インフルエンザ菌、モラクセラ・カタラーリス、マイコプラズマ・トラコマチス。試験管内および臨床研究により、アジスロマイシンは、細胞内マイコバクテリウム複合体(鳥型結核菌および細胞内マイコバクテリウムからなる)によって引き起こされる疾患を予防できることが確認されています。アジスロマイシンは、ベータラクタマーゼを産生する菌株に対しては効果がありません。アジスロマイシンは、次の微生物に対してin vitroで抗菌効果があることが研究により示されていますが、その臨床的意義は、Streptococcus mutans、Bordetella pertussis、Haemophilus ducrei、Legionella pneumophilaなど、その臨床的意義はまだ不明です、バクテロイデス、肺炎連鎖球菌、ボレリア、肺炎クラミジア、梅毒トレポネーマ、ウレアプラズマ・ウレアリティカムなど。
使用法と投与量
この製品は、水で直接飲み込むか、適量の温水に入れてよくかき混ぜてから摂取することができます(詳細については、手順を参照してください)。
処方
分散性フィルム
仕様書
0.25g
取扱説明書
承認日2007年5月8日
改訂日2010年10月1日
2013年12月11日2015年11月25日、パッケージ仕様の増加
アジスロマイシン分散錠
指示を注意深く読み、医師の指導の下で使用してください。
[薬の名前]
一般名:アジスロマイシン分散錠
製品名:ジュン・ジェ
英語名:Azithromycin Dispersible Tablets
中国語ピンイン:Aqimeisu Fensanpian
[成分]この製品の主な成分はアジスロマイシンです。
化学名:(2R、3S、4R、5R、8R、10R、11R、12S、13S、14R)-13-[(2,6-ジデオキシ-3-C-メチル-3-O-メチル- α-L-核-ヘキシラノシル)オキシ] -2-エチル-3,4,10-トリヒドロキシ-3,5,6,8,10,12,14-ヘプタメチル-11- [ [3,4,6、-トリデオキシ-3-(ジメチルアミノ)-β-D-ウッド-ピラノシル]オキシ] -1-オキサ-6-アザシクロペンタデカン-15オン 。
化学構造:
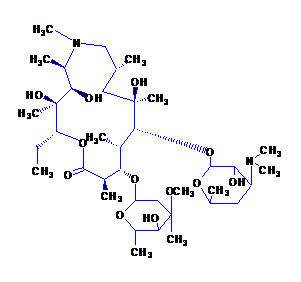
分子式:C38H72N2O12
分子量:749.00
【特性】本製品は白色またはオフホワイトです。
[適応]この製品は、敏感な細菌によって引き起こされる以下の感染症に適しています。
中耳炎、副鼻腔炎、咽頭炎、扁桃炎などの上気道感染症、気管支炎や肺炎などの下気道感染症。皮膚および軟部組織感染症、クラミジアトラコマチスによる単純性器感染症、非多剤耐性resistant菌による単純性器感染症(メルファラン種の組換え感染症)。
【仕様】0.25g
[使用量と投与量]感染症の治療、治療と使用のコースのためのアジスロマイシン錠剤は次のとおりです。
この製品は、水で直接飲み込むか、適量の温水に入れてよく混ぜてから摂取できます。
成人:クラミジアトラコマチスまたは敏感な菌によって引き起こされる性感染症。1.0g(4錠)のこの製品を単回投与するだけですみます。
その他の感染症の治療:総投与量は1.5g(6錠)で、1日1回この製品を0.5g(2錠)の3回に分けます。または、総投与量は同じで、1.5g(6錠)、1日目に0.5g(2錠)を服用し、1日1回0.25g(1錠)を2〜5日目に服用します。
【副作用】
(1)臨床試験の経験
臨床試験はさまざまな条件下で行われるため、臨床試験で観察された1つの薬物の有害反応率は、臨床試験の他の薬物の有害反応率と直接比較することはできず、実際の用途での有害反応を反映しない場合があります。レート。
市中肺炎に対するアジスロマイシン静脈内製剤の臨床試験では、2〜5回の用量が静脈内投与され、報告された副作用のほとんどは軽度から中等度であり、薬物の中止後に回復しました。これらの臨床試験のほとんどの患者には複数の併存疾患があり、他の薬物を適用する必要があります。この製品の静脈内注射を受けた患者の約1.2%は薬物を中止し、静脈内または経口アジスロマイシンで治療された患者の2.4%は有害反応症状または異常な臨床検査のために投薬を中止しました。
骨盤内炎症性疾患の患者を対象とした臨床試験では、アジスロマイシン単剤療法を受けた患者の2%が静脈内薬剤投与を受け、臨床的副作用により中止された患者の2%、アジスロマイシンとメトロニダゾールの患者が患者の4%が副作用のために治療を中止しました。
上記の研究では、薬物の中止に至る最も一般的な副作用は胃腸反応(腹痛、吐き気、嘔吐、下痢など)および発疹であり、アミノトランスフェラーゼおよび/またはアルカリホスファターゼの中止のための異常な臨床検査に至りました。高い。
市中感染肺炎の研究では、静脈/経口製剤を投与されている成人患者で最も一般的な副作用は、下痢または軟便(4.3%)、悪心(3.9%)、腹痛(2.7)などの胃腸反応でした。 %)、嘔吐(1.4%)。患者の約12%は静脈注射に関連した副作用を有し、最も一般的なものは注射部位の痛み(6.5%)および局所炎症反応(3.1%)です。
骨盤内炎症性疾患の患者の臨床試験では、成人女性患者に本製品の静脈内/経口製剤が投与されます。治療に関連する最も一般的な副作用は胃腸反応で、その中でも下痢(8.5%)と吐き気(6.6)が一般的です。 %)、膣炎(2.8%)、腹痛(1.9%)、食欲不振(1.9%)、発疹とかゆみ(1.9%)が続きます。これらの研究において、アジスロマイシンとメトロニダゾールの組み合わせは、吐き気(10.3%)、腹痛(3.7%)、嘔吐(2.8%)、投与部位、口内炎、めまい、呼吸困難の女性患者の高い割合で発生しました。 1.9%)。
アジスロマイシンの静脈内/経口多回投与レジメンによって引き起こされる他の有害反応は、1%を超えませんでした。
発生率1%以下の副作用は次のとおりです。
胃腸反応:消化不良、鼓腸、粘膜炎、口腔カンジダ症および胃炎。
神経系:頭痛、嗜眠。
アレルギー反応:気管支痙攣。
特別な感じ:味が間違っています。
(II)上場後の申請後の経験
経口アジスロマイシン製剤は、市販後の成人および/または小児患者に使用され、次の有害事象の報告がありますが、アジスロマイシンが原因かどうかは定かではありません。
アレルギー:関節痛、浮腫、ur麻疹、血管浮腫。
心血管系:不整脈には、心室頻拍、低血圧、まれなQT間隔の延長、および心室頻拍のトルサードが含まれます。
消化管:食欲不振、便秘、消化不良、腹部膨満、嘔吐/下痢はまれですが、脱水、偽膜性大腸炎、膵炎、口腔カンジダ症、幽門狭窄、まれな舌の変色はほとんど起こりません。
全身反応:疲労、感覚異常、疲労、不快感、およびアナフィラキシーショック反応。
泌尿生殖器系:間質性腎炎、急性腎不全、膣炎。
造血系:血小板減少症。
肝臓/胆道:肝機能障害に関連する副作用は、販売後のアジスロマイシンの経験で報告されています。
神経系:けいれん、めまい/めまい、頭痛、嗜眠、多動、緊張、動揺、失神。
異常な耳と失われた:難聴、耳鳴り、難聴、めまい。
精神:攻撃的な反応と不安。
皮膚と付属品:かゆみ、多発性紅斑、スティーブンスジョンソン症候群、中毒性表皮壊死などのまれで重度の皮膚反応。
特別な感覚:聴覚障害には、難聴、難聴および/または耳鳴り、ならびに味覚/嗅覚異常および/または喪失の報告が含まれます。
検査室検査異常:
臨床試験で見られる重要な臨床検査(薬物に関連するかどうか)は次のとおりです。
発生率は4%〜6%です:アラニンアミノトランスフェラーゼ(ALT)、アスパラギン酸アミノトランスフェラーゼ(AST)、およびクレアチニン。
発生率は1%〜3%です:乳酸脱水素酵素(LDH)とビリルビンが上昇しています。
発生率は1%未満です:白血球減少症、好中球減少症、血小板数の減少、および血清アルカリホスファターゼの上昇。
フォローアップにより、上記の検査室の異常は可逆的であることがわかった。
750人以上の患者を対象としたアジスロマイシンの複数回投与(静脈内/経口)の臨床試験では、治療関連の肝酵素の異常によりアジスロマイシンを中止した患者は2%未満です。
[タブー]
アジスロマイシン、エリスロマイシン、他のマクロライドまたはケトリドにアレルギーのある患者では禁止されていることが知られています。アジスロマイシンの使用後に胆汁うっ滞性黄und /肝機能障害の既往がある患者は以前禁止されていました。
警告
アレルギー反応
血管浮腫、アナフィラキシーショック、スティーブンスジョンソン症候群や中毒性表皮壊死症などの皮膚反応を含む重度のアレルギー反応の報告は、アジスロマイシンによる治療ではまれです。まれですが、死の報告があります。一部の患者では、アレルギー症状は最初に対症療法が行われますが、アジスロマイシンを使用しなくても治療が時期尚早に中止されると、アレルギー症状はすぐに再発する可能性があります。そのような患者の対症療法と観察の時間を延長する必要があります。これらのイベントの発生が、組織内のアジスロマイシンの長い半減期と、抗原への身体のより長い暴露に関連しているかどうかは不明です。
アレルギー反応が発生した場合、薬物は直ちに中止し、適切な治療を行う必要があります。医師は、対症療法を停止した後にアレルギー症状が再び現れる場合があることを知っておく必要があります。
肝毒性
異常な肝機能、肝炎、黄undの胆汁うっ滞、肝壊死、肝不全の報告があり、そのいくつかは致命的かもしれません。肝炎の症状と徴候が現れた場合は、すぐにこの製品の使用を中止してください。
クロストリジウム・ディフィシル関連下痢
ほぼすべての抗菌薬には、この製品を含むクロストリジウムディフィシル関連下痢(CDAD)の報告があります。これは、軽度の下痢から致命的な大腸炎までさまざまです。抗菌処理は、結腸の正常な植物相に変化を引き起こし、クロストリジウムディフィシルの過剰な繁殖を引き起こす可能性があります。
クロストリジウム・ディフィシルによって産生される毒素Aおよび毒素Bは、CDADの病因と関連しています。高毒性のC.ディフィシルは罹患率と死亡率の増加を引き起こし、これらの感染症は抗生物質による治療が難しく、結腸切除が必要になる場合があります。抗生物質を使用した後の下痢のすべての患者については、CDADの可能性を考慮しなければなりません。 2か月以上の抗生物質治療後にCDADの報告があったため、病歴について慎重に尋ねる必要があります。
CDADが疑われるか診断された場合、クロストリジウムディフィシルに使用されていない抗生物質を中止する必要があるかもしれません。水、電解質、およびタンパク質は、臨床ニーズに応じて適切に補充する必要があり、クロストリジウムディフィシルに対して有効な抗生物質を投与し、必要に応じて外科的評価を実施する必要があります。
【注意事項】
一般:アジスロマイシンは主に肝臓で除去されるため、肝機能障害のある患者はアジスロマイシンを慎重に使用する必要があります。 GFR <10 mL / minの被験者のデータは限られているため、このような患者にはアジスロマイシンを注意して使用する必要があります。異常な肝機能、肝炎、胆汁うっ滞性黄und、肝壊死、肝不全の報告があり、そのいくつかは致命的かもしれません。肝炎の兆候や症状がある場合は、アジスロマイシンを直ちに中止する必要があります。
QT間隔の延長
アジスロマイシンを含む他のマクロライド系抗生物質の使用は、心室の再分極とQT間隔の延長を引き起こし、不整脈のリスクと心室性頻拍を引き起こすことが報告されています。アジスロマイシンを服用している患者の市販後調査では、トルサードドポアント心室頻拍の症例の自発的な報告がありました。リスクの高い集団でアジスロマイシンを使用するリスクと利点を比較検討する場合、医療提供者は次のような致命的なQT間隔延長のリスクを考慮する必要があります。
· QT間隔の延長、トキソプラズマ性トルサード心室頻拍、先天性QT延長症候群、徐脈性不整脈または非代償性心不全の患者が知られています。
· 抗精神病薬、抗うつ薬、フルオロキノロンなど、QT間隔の薬を延長することが知られている患者。
· 未補正の低カリウム血症または低マグネシウム血症などの不整脈、臨床的に有意な徐脈、およびIA型(キニジン、プロカインアミド)およびIII型( ドフェチリド、アミオダロン、ソタロールなどの抗不整脈薬の患者。
· 高齢患者:高齢患者は、薬物関連のQT間隔の影響に対してより敏感になる場合があります。
アジスロマイシン治療を受けた患者は、重症筋無力症または新しい重症筋無力症症候群の悪化を報告しています。
診断がない場合、または細菌感染が疑われる場合、または予防の兆候がない場合、この製品の使用は患者にとって有益ではない可能性があり、薬剤耐性菌のリスクが高まります。
患者は知る必要があります:
アジスロマイシンは、アレルギー反応の兆候が生じたらすぐに中止し、医師に連絡してください。
この製品(アジスロマイシン)を含む抗生物質は細菌感染症の治療にのみ使用でき、ウイルス感染症(風邪など)の治療には使用できないことを患者に通知する必要があります。この製品(アジマイシン)を使用して細菌感染症を治療する場合、患者は通常、治療の開始時に気分が良くなりますが、正確な投薬については医師の指示に従う必要があることを通知する必要があります。治療の全過程が欠落しているか、完了していない可能性があります:(1)現在の治療の有効性を低下させます;(2)アジスロマイシンまたは他の抗生物質が将来これらの耐性菌を治療することができなくなる細菌耐性の可能性を高めます
抗生物質による治療はしばしば下痢を引き起こし、通常下痢は抗生物質を止めた後に回復します。抗生物質治療後、患者は最後の抗生物質使用の2か月以上後に、水様便または血便(胃けいれんおよび発熱を伴うまたは伴わない)を経験することがあります。この場合、患者はできるだけ早く医師に連絡する必要があります。
[妊娠中の女性と授乳中の女性]
動物の生殖毒性研究は、アジスロマイシンが胎盤を通過するが、敷料への損傷の兆候を示さないことを示しています。母乳にはこの製品の分泌データはありません。動物試験データは、人間の適用を完全には予測していません。妊娠および授乳における使用の安全性はこれまで確認されていないため、妊娠中または授乳中の女性に適した選択肢がない場合、この製品は使用しないでください。
[子供用医薬品]この実験は実施されておらず、信頼できる基準はありません。
[老人用]この実験は実施されておらず、信頼できる基準はありません。
[薬物相互作用]
薬物相互作用:ネルフィナビルの定常状態でのアジスロマイシンの単回投与の経口投与は、アジスロマイシンの血清濃度を増加させる可能性があります。ネルフィナビルと組み合わせて使用する場合、アジスロマイシンの投与量を調整する必要はありませんが、肝酵素の異常や聴覚障害などのアジスロマイシンの既知の副作用を注意深く監視する必要があります。
自発的な市販後報告は、アジスロマイシンの併用が経口抗凝固薬の効果を高める可能性があることを示唆しています。患者がアジスロマイシンおよび経口抗凝固薬と併用される場合、プロトロンビン時間を厳密に監視する必要があります。
治療用量で、アジスロマイシン対アトルバスタチン、カルバマゼピン、セチリジン、ジダノシン、エファビレンツ、フルコナゾール、インジナビル、ミダゾラム、リファブチン、西ジピリダモール、テオフィリン(静脈内および経口投与)、トリアゾラム、トリメトプリム/スルファメトキサゾールまたはジドブジンの薬物動態はほとんど効果がありません。併用すると、エファビレンツまたはフルコナゾールはアジスロマイシンの薬物動態にほとんど影響しません。アジスロマイシンを上記の薬剤のいずれかと組み合わせる場合、いずれかの薬剤の用量を調整する必要はありません。
アジスロマイシンは、臨床試験で以下の薬剤と相互作用すると報告されていません。しかし、アジスロマイシンとこれらの薬物との潜在的な相互作用を評価するための特定の研究はこれまで行われていません。ただし、これらの条件は、他のマクロライドが使用されたときに発生しました。したがって、新しい研究データがない場合、アジスロマイシンは以下の薬剤と併用した場合に注意深く観察する必要があります。
ジゴキシン-ジゴキシゲニンの血中濃度が増加しました。
エルゴサミンまたはジヒドロエルゴタミン-重度の末梢血管攣縮および感覚異常として現れる急性麦角中毒。
テルビナジン、シクロスポリン、ヘストベータおよびフェニトインの濃度が上昇しました。
臨床検査への影響:臨床検査への影響の報告は報告されていません。
[薬物の過剰摂取]薬物の過剰摂取の悪影響は、推奨される用量と同じです。過剰使用が発生すると、胃洗浄や一般的な支持療法などの症状に応じて対症療法と支持療法を行うことができます。
【薬理学と毒性学】
薬理作用
アジスロマイシンは、感受性の高い微生物の50代リボソームのサブユニットに結合することにより、タンパク質の合成を(核酸の合成に影響を与えることなく)阻害する作用機構を持つアザライド系抗生物質です。
試験管内および臨床研究の両方で、アジスロマイシンはさまざまな病原菌に対して抗菌効果があることが示されています。
グラム陽性好気性微生物:黄色ブドウ球菌、化膿連鎖球菌、肺炎連鎖球菌、溶血性連鎖球菌。
アジスロマイシンは、エリスロマイシン耐性グラム陽性菌に対して交差耐性です。大部分の連鎖球菌(腸球菌)およびメチシリン耐性ブドウ球菌は、この製品に耐性があります。
グラム陰性好気性微生物:インフルエンザ菌、モラクセラ・カタラーリス、マイコプラズマ・トラコマチス。
試験管内および臨床研究により、アジスロマイシンは細胞内マイコバクテリウム複合体(鳥型結核菌と細胞内マイコバクテリウムからなる)によって引き起こされる疾患を予防できることが確認されています。
アジスロマイシンは、ベータラクタマーゼを産生する菌株に対しては効果がありません。
アジスロマイシンは、次の微生物に対してin vitroで抗菌効果があることが研究により示されていますが、その臨床的意義は、Streptococcus mutans、Bordetella pertussis、Haemophilus ducrei、Legionella pneumophilaなど、その臨床的意義はまだ不明です、バクテロイデス、肺炎連鎖球菌、ボレリア、肺炎クラミジア、梅毒トレポネーマ、ウレアプラズマ・ウレアリティカムなど。
毒性研究
遺伝毒性ヒトリンパ球アッセイ、マウス骨髄小核アッセイ、およびマウスin vitroリンパ腫細胞アッセイの結果アジスロマイシンは変異原性を示さなかった。
生殖毒性ラットおよびマウスの生殖毒性試験により、アジスロマイシン(経口投与)の用量は、中程度の母体毒性を生じる用量レベルに達することが示されています(すなわち、200 mg / kg /日、体表面積に基づいて約500 mgのヒト用量) / kg / dayが2〜4倍の場合、催奇形性効果は観察されませんでした。
生殖能力と胎児への損傷は発見されていません。現在、妊婦を対象とした適切かつ厳密な対照臨床試験はありません。動物の生殖研究の結果は常に人間の状態を予測するものではないため、アジスロマイシンは本当に必要な場合にのみ妊婦が使用できます。多くの薬物は母乳によって分泌されるため、母乳で育てる女性は使用する際に注意する必要があります。
発がん性アジスロマイシン動物の長期使用の発がん性に関する研究はありません。
[薬物動態]
経口投与後に急速に吸収され、37%の生物学的利用能があります。経口0.5 gの単回投与後、ピーク時間は2.5〜2.6時間で、ピーク血漿濃度(Cmax)は0.4〜0.45 mg / Lです。この製品は体内に広く分布しており、各組織の濃度は同じ期間に血中濃度の50倍に達し、マクロファージと線維芽細胞の濃度が高く、前者はアジスロマイシンを炎症部位に運ぶことができます。単剤投与後の血中排泄半減期(T1 / 2)は35〜48時間であり、投与量の50%以上が元の形で胆道を介して排出され、元の形の約4.5%が投与後72時間以内に尿を介して排出されます。本製品の血清タンパク質結合率は、血中濃度の増加とともに低下します。血中濃度が0.02μg/ mlの場合、血清タンパク質結合率は15%、血中濃度が2μg/ mlの場合、血清タンパク質結合率は7%。食物は、この製品の生物学的利用能に影響しません。
[保管]遮光、密閉、乾燥した場所での保管。
[包装]アルミプラスチック包装、6個/箱、12個/箱。
[有効期間] 24か月。
[実行基準] 2010年版中国薬局方の第2版。
[承認番号] National Drug Standard H20020729。
[メーカー]
会社名:Lunan Beite Pharmaceutical Co.、Ltd.
生産住所:山東省臨y市銀que山路243号
郵便番号:276006
電話番号:0539-8336336(販売)0539-8336337(品質パイプ部門)
FAX番号:0539-8336029(販売)0539-8336338(品質パイプ部門)
ウェブサイト:www.LUNAN.com.cn
24時間対応のカスタマーサービスホットライン:400-0539-310

