ロスバスタチンカルシウム錠
適応症
この製品は、食餌療法やその他の非薬物療法(運動療法、減量など)によって適切に管理されていない原発性高コレステロール血症(ヘテロ接合型家族性高コレステロール血症を含むIIa型)に適しています。混合型脂質異常症(タイプIIb)。この製品は、食事管理やその他の脂質低下対策(LDL除去療法など)の補助として、またはこれらの方法が適用できない場合に、ホモ接合型家族性高コレステロール血症の患者にも適しています。
臨床薬理学
ロスバスタチンは、選択的で競合的なHMG-CoAレダクターゼ阻害剤です。 HMG-CoAレダクターゼは、3-ヒドロキシ-3-メチルグルタリル補酵素Aをコレステロールの前駆体であるメバロン酸に変換する際の律速酵素です。動物実験と細胞培養試験の結果は、ロスバスタチンが肝臓において高度かつ高度に選択的であり、肝臓がコレステロールを下げるための標的器官であることを示しています。生体内および生体外の試験により、ロスバスタチンは細胞表面の肝LDL受容体の数を増加させ、それによりLDLの取り込みと異化を促進し、肝臓VLDL合成を阻害し、それによりVLDLおよびLDL粒子の総数を減らすことが示されましたホモ接合およびヘテロ接合の家族性高コレステロール血症患者、非家族性高コレステロール血症患者、混合脂質異常症患者の場合、ロスバスタチンは総コレステロール、LDL-C、ApoB、非HDL-Cレベルを低下させることができます。また、ロスバスタチンはTGを低下させ、HDL-Cレベルを上昇させます。高トリグリセリド血症のみの患者では、ロスバスタチンは総コレステロール、LDL-C、VLDL-C、ApoB、非HDL-C、TGレベル、およびHDL-Cレベルの上昇を減少させました。ロスバスタチンが心血管系の罹患率と死亡率に及ぼす影響は明らかにされていません。
使用法と投与量
患者は、治療開始前に標準的なコレステロール低下食管理を行い、治療中は食事管理を維持する必要があります。この製品の使用は、個人のコレステロールレベル、予想される心血管リスクおよび副作用の潜在的リスクを考慮して、個別化の原則に従う必要があります...(指示を参照)
処方
タブレット
仕様書
(1)5 mg;(2)10 mg;(3)20 mg
取扱説明書
承認日:2008年5月4日
改訂日:2012年3月13日
2013年12月10日
ロスバスタチンカルシウム錠の指示
指示を注意深く読み、医師の指導の下で使用してください。
[薬の名前]
一般名:ロスバスタチンカルシウム錠
英語名: Rosuvastatin Calcium Tablets
中国語ピンイン: Ruishufatatinggai Pian
[成分]この製品の主な成分はロスバスタチンカルシウムです。
化学名:ビス-[(E)-7- [4-(4-フルオロフェニル)-6-イソプロピル-2- [メチル(メチルスルホニル)アミノ]-ピリミジン-5-イル]( 3R、5S)-3,5-ジヒドロキシヘプト-6-エン酸]カルシウム塩(2:1)
化学構造:
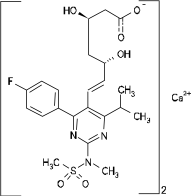
分子式:(C22H27FN3O6S)2Ca 分子量:1001.15
【特性】本製品はフィルムコーティング錠で、コーティングを除去すると白色またはオフホワイトになります。
[適応]
この製品は、食餌療法やその他の非薬物療法(運動療法、減量など)によって適切に管理されていない原発性高コレステロール血症(ヘテロ接合型家族性高コレステロール血症を含むIIa型)に適しています。混合型脂質異常症(タイプIIb)。
この製品は、食事管理やその他の脂質低下対策(LDL除去療法など)の補助として、またはこれらの方法が適用できない場合に、ホモ接合型家族性高コレステロール血症の患者にも適しています。
[仕様]ロスバスタチンによる(C22H27FN3O6S)
(1)5 mg;(2)10 mg;(3)20 mg
[用法・用量]
患者は、治療開始前に標準的なコレステロール低下食管理を行い、治療中は食事管理を維持する必要があります。この製品の使用は、個人のコレステロールレベル、予想される心血管リスク、副作用の潜在的リスクを考慮して、個別化の原則に従う必要があります。
経口。この製品は通常、1日1回5mgの開始用量で使用されます。開始用量の選択は、個人の個々のコレステロール値、予想される心血管リスク、および副作用の潜在的リスクを考慮に入れる必要があります。 LDL-C(LDL-C)をより効果的に下げる必要がある患者の場合、1日1回10 mgを開始用量と見なすことができ、ほとんどの患者の血中脂質レベルを制御できます。必要に応じて、治療の4週間後に用量をより高いレベルに調整できます。この製品の最大1日量は20mgです。
この製品は一日中いつでも投与でき、食事中または空腹時に摂取できます。
腎不全薬の患者
軽度および中等度の腎障害がある患者は、用量を調整する必要はありません。この製品のすべての用量は、重度の腎機能障害のある患者には禁忌です。
肝障害患者の薬物使用
Child-Pughスコアが7以下の被験者では、ロスバスタチンへの全身暴露は上昇しませんでした。 Child-Pughスコアが8および9の被験者では、全身暴露の増加が観察されました。これらの患者では、腎機能の評価を考慮する必要があります。 Child-Pughスコアが9を超える患者でこの製品を使用した経験はありません。この製品は、活動性肝疾患の患者には禁忌です。
人種
アジアの被験者の全身暴露の増加が観察されています。アジア系の患者の線量を決定する際には、この要因を考慮する必要があります。
【副作用】
この製品で見られる副作用は通常、軽度で一時的なものです。海外の対照臨床試験では、有害事象のために試験を中止した患者は4%未満でした。
有害事象の頻度は、一般的(発生率> 1/100、<1/10)、まれ(> 1/1000、<1/100)、まれ(> 1/10000、<1/1000)、非常にまれです(<10000)。
免疫系異常
まれ:血管性浮腫を含むアレルギー反応。
神経系異常
共通:頭痛、めまい
異常な消化管
共通:便秘、吐き気、腹痛
異常な皮膚および皮下組織
まれ:かゆみ、発疹、ur麻疹
骨格筋、関節および骨の異常
共通:筋肉痛
まれ:ミオパチーと横紋筋融解症
異常な体
共通:無力
他のHMG-CoAレダクターゼ阻害剤と同様に、この製品での副作用の発生率は、用量の増加とともに増加する傾向があります。
腎臓への影響:この製品を投与された患者では、タンパク尿(テストストリップテスト)が観察され、タンパク質の大部分は腎尿細管に由来していました。患者の約1%が、10 mgおよび20 mgの治療期間中にタンパク尿が++以上に増加しないか、最小限に増加しました。これは、40 mgの治療を受けた患者では約3%でした。 20 mgの用量治療では、タンパク尿の増加がゼロまたはわずかに増加したことが観察されました。ほとんどの場合、タンパク尿は治療を続けると自動的に減少または消失します。
骨格筋への影響:筋肉痛、ミオパシー、まれな横紋筋融解症など、さまざまな用量のこの製品を投与されている患者、特に20 mgを超える用量の患者の骨格筋への影響の報告があります。 。
この製品を服用している患者では、クレアチンキナーゼ(CK)のレベルの上昇が用量依存的であることが観察されました;ほとんどの症例は軽度、無症候性、一過性でした。 CKレベルが上昇した場合(> 5 x ULN)、治療を中止する必要があります。
肝臓への影響:他のHMG-CoAレダクターゼ阻害剤と同様に、この製品を服用している少数の患者で用量に関連したトランスアミナーゼの上昇が観察されました;ほとんどの症例は軽度、無症候性、一過性でした。
市販後の経験:スタチンの市販後モニタリングには、高血糖、耐糖能異常、糖化ヘモグロビン値の上昇、糖尿病の発症、血糖コントロールの悪化の報告があり、一部のスタチンには低血糖の報告があります。
スタチンの市販後サーベイランスには、記憶喪失、記憶喪失、混乱などの認知機能障害のまれなケースがあり、ほとんどは重篤ではない可逆的な反応であり、薬物を停止した後に回復できます。
上記の反応に加えて、この製品の市販後使用中に以下の有害事象が報告されました。
肝胆道疾患:
非常にまれ:黄und、肝炎;
まれ:肝トランスアミナーゼの上昇。
筋骨格障害:
まれ:関節痛
神経系疾患:
非常にまれ:多発神経障害
[タブー]
この製品は禁止されています:
● ロスバスタチンまたはこの製品の成分のいずれかにアレルギーがある人。
● 原因不明の血清トランスアミナーゼ値の上昇および正常値の上限(ULN)の3倍を超える血清トランスアミナーゼ値の上昇を含む、活動性肝疾患の患者。
● 重度の腎機能障害の患者(クレアチニンクリアランス<30 ml /分)。
● ミオパチーの患者。
● シクロスポリンを同時に使用する患者。
● 妊娠中、授乳中、および適切な避妊なしで妊娠する可能性が高い女性。
【注意事項】
腎臓への影響
高用量、特に40 mgで治療された患者では、タンパク尿(テストストリップテスト)が観察され、タンパクの大部分は腎尿細管に由来していました。
骨格筋への影響
筋肉痛、ミオパチー、まれな横紋筋融解症など、この製品をさまざまな用量で投与している患者、特に20 mgを超える用量の患者の骨格筋への影響が報告されています。
クレアチンキナーゼアッセイ
クレアチンキナーゼ(CK)は、激しい運動の後、または結果の解釈を混乱させるCK上昇を引き起こすもっともらしい要因の存在下で検出されるべきではありません。 CK基準値が大幅に増加した場合(> 5×ULN)、テストは5〜7日以内に確認する必要があります。 繰り返しテストを行って、患者のCKベースライン値が5 x ULNより大きいことが確認された場合、治療を開始できません。
治療前
他のHMG-CoAレダクターゼ阻害剤と同様に、この製品を使用する場合、ミオパシー/ラブドミン感受性の患者は注意が必要です。
これらの要因は次のとおりです。
● 腎機能障害
● 甲状腺機能低下症
● 私または家族の歴史における遺伝性筋疾患
● 他のHMG-CoAレダクターゼ阻害剤またはフィブラートの筋肉毒性の過去の履歴
● アルコール乱用
● 年齢> 70歳
● 血中濃度の増加の可能性
● Bateクラスを同時に使用する
これらの患者については、治療の潜在的な利益と潜在的なリスクとの関係を考慮すべきであり、臨床モニタリングが推奨されます。患者のCKベースライン値が著しく高い場合(> 5 x ULN)、治療を開始しないでください。
治療中
特に不快感や発熱を伴う場合は、原因不明の筋肉痛、筋力低下、または痙攣を直ちに報告するよう患者に求める必要があります。これらの患者は、CKレベルをテストする必要があります。 CK値が著しく高い場合(> 5 x ULN)、または筋肉の症状がひどく1日を通して不快感を引き起こす場合(CK≤5 x ULNであっても)、治療を中止する必要があります。症状が解消され、CKレベルが正常に戻った場合は、製品の再投与または他のHMG-CoAレダクターゼ阻害剤の最低用量への切り替えを検討し、注意深く観察してください。
無症候性患者のCKレベルの定期的な検査は必要ありません。
臨床研究では、この製品と他の治療を使用する少数の患者で骨格筋に対する薬物の効果が増加するという証拠はありません。しかし、他のHMG-CoAレダクターゼ阻害剤およびベリリック酸誘導体(ゲムフィブロジルを含む)、シクロスポリン、ニコチン酸、アゾール抗真菌剤、プロテアーゼ阻害剤、またはマクロライド系抗生物質が発見されました筋炎とミオパシーの発生率は、併用された患者で増加しました。ゲムフィブロジルは、筋障害のリスクを高めるために、いくつかのHMG-CoAレダクターゼ阻害剤と組み合わせて使用されます。したがって、この製品は、ゲムフィブロジルとの併用は推奨されていません。脂質レベルとこの組み合わせの潜在的なリスクをさらに改善するために、フィブラートまたはナイアシンと組み合わせてこの製品の利点を比較検討する必要があります。
ミオパシーに関連する急性または重度の腎不全(敗血症、低血圧、大手術、外傷、重度の代謝、内分泌および電解質異常、または制御不能のてんかんなど)この製品は患者には使用できません。
肝臓への影響
他のHMG-CoAレダクターゼ阻害剤と同様に、この製品は過剰なアルコールおよび/または肝疾患の患者には注意して使用する必要があります。治療を開始する前と開始後3ヶ月で肝機能検査を行うことをお勧めします。血清トランスアミナーゼが正常の上限の3倍を超えて上昇する場合、この製品は中止または削減する必要があります。
甲状腺機能低下症またはネフローゼ症候群に続発する高コレステロール血症の場合、この製品による治療を開始する前に原発疾患を治療する必要があります。
人種
薬物動態学的研究は、アジア人の被験者が白人よりも高い曝露をしていることを示しています。
運転車両と機械の操作への影響
この製品が自動車の運転や機械の操作に与える影響を判断するための研究は行われていません。ただし、薬力学的特性によっては、この製品がこれらの機能に影響を与えることはほとんどありません。車両を運転して機械を操作するとき、治療中にめまいが発生する可能性があることを考慮する必要があります。
[妊娠中の女性と授乳中の女性]
この製品は、妊婦および授乳中の女性には禁忌です。
妊娠する可能性が高い女性は、適切な避妊手段を講じる必要があります。
コレステロールおよびその他のコレステロール生合成産物は胚の発生に重要であるため、HMG-CoAレダクターゼによる阻害のリスクは妊婦の治療の利点を上回ります。動物実験は、生殖毒性が限られていることの証拠を提供します。この製品の使用中に患者が妊娠している場合は、治療を直ちに中止する必要があります。ロスバスタチンはラットのミルクに分泌されます。ロスバスタチンの母乳への分泌に関する情報はありません。
[子供の薬]
この製品の子供に対する安全性と有効性は確立されていません。小児での使用経験は、同型接合の家族性高コレステロール血症の少数の子供(8歳以上)に限られています。したがって、小児科医がこの製品を使用することは現在推奨されていません。
[老人用]
用量を調整する必要はありません。
[薬物相互作用]
シクロスポリン:シクロスポリンと組み合わせて使用した場合、ロスバスタチンのAUCは、健康なボランティアで観察されたAUCよりも7倍高かった(この製品の同じ用量と比較して)。併用は、シクロスポリンの血漿濃度に影響しません。
ビタミンK拮抗薬:他のHMG-CoAレダクターゼ阻害剤と同様に、ビタミンK拮抗薬(例:ワルファリン)で患者を開始するか、用量を徐々に増やすと、INRが増加する場合があります。この製品を無効にするか、この製品の用量を徐々に減らすと、INRが減少する可能性があります。この場合、INRを適切に検出する必要があります。
ゲムフィブロジルおよびその他の脂質低下製品:この製品をゲムフィブロジルと組み合わせて使用すると、ロスバスタチンのCmaxおよびAUCを2倍に増やすことができます。
特殊な相互作用研究のデータに基づいて、この製品は薬物動態なしでフェノフィブラートと相互作用すると予想されますが、薬力学的相互作用が発生する可能性があります。
ゲムフィブロジル、フェノフィブラート、他のフィブラートおよびナイアシンの脂質低下用量(≥1g/日)とHMG-CoAレダクターゼ阻害剤を併用すると、ミオパシーのリスクが高まります。投与すると筋障害を引き起こす可能性があります。
制酸剤:この製品と水酸化マグネシウムアルミニウムを含む制酸剤懸濁液の同時投与により、ロスバスタチンの血漿濃度が約50%減少しました。この製品を服用してから2時間後に制酸剤を投与すると、効果が緩和されます。この薬物相互作用の臨床的意義は研究されていません。
エリスロマイシン:この製品とエリスロマイシンを併用すると、ロスバスタチンのAUC(0-t)が20%減少し、Cmaxが30%減少しました。この相互作用は、エリスロマイシンによって引き起こされる胃腸運動性の増加による可能性があります。
経口避妊薬/ホルモン補充療法(HRT):この製品と経口避妊薬の使用により、エチニルエストラジオールとノルゲストレルのAUCがそれぞれ26%と34%増加しました。経口避妊薬の用量を選択するときは、血中濃度のこれらの増加を考慮する必要があります。この製品とHRTの両方を使用する被験者の薬物動態データはないため、同様の相互作用を排除することはできません。しかし、臨床試験では、この組み合わせは広く利用可能であり、患者によく許容されています。
その他の薬物:特殊な薬物相互作用研究のデータに基づいて、この製品とジゴキシンの間に臨床的に関連する相互作用はないと推定されています。
チトクロームP450酵素:in vitroおよびin vivoの両方の研究により、ロスバスタチンは細胞P450アイソザイムの阻害剤でも酵素誘導物質でもないことが示されています。さらに、ロスバスタチンはこれらの酵素の弱い基質です。ロスバスタチンとフルコナゾール(CYP 2CPおよびCYP 3A4の阻害剤)またはケトコナゾール(CYP 2A6およびCYP 3A4の阻害剤)の間に臨床的に関連する相互作用はありません。イトラコナゾール(CYP 3A4の阻害剤)と組み合わせて、ロスバスタチンのAUCは28%増加しましたが、この増加は臨床的に有意とは見なされませんでした。したがって、シトクロムP450を介した代謝による薬物相互作用はないと推定されます。
プロテアーゼ阻害剤:薬物相互作用のメカニズムは明確ではありませんが、プロテアーゼ阻害剤の同時投与により、ロスバスタチンの暴露が大幅に増加する可能性があります。薬物動態研究では、この製品20 mgと2つのプロテアーゼ阻害剤(ロピナビル400 mg /リトナビル100 mg)の組み合わせを摂取した健康なボランティアが、ロスバスタチンの定常状態AUCを示しました( 0-24)およびCmaxはそれぞれ約2倍および5倍増加しました。したがって、プロテアーゼ阻害剤で治療されているHIV患者にこの製品を使用することは推奨されません。
【薬物の過剰摂取】
この製品が過剰摂取された場合、特別な治療はありません。過剰摂取が発生したら、対症療法を行い、必要に応じて支援策を講じる必要があります。肝機能とCKレベルを監視する必要があります。血液透析は有意な効果をもたらさないかもしれません。
【薬理学と毒性学】
薬理作用
ロスバスタチンは、選択的で競合的なHMG-CoAレダクターゼ阻害剤です。 HMG-CoAレダクターゼは、3-ヒドロキシ-3-メチルグルタリル補酵素Aをコレステロールの前駆体であるメバロン酸に変換する際の律速酵素です。動物実験と細胞培養試験の結果は、ロスバスタチンが肝臓において高度かつ高度に選択的であり、肝臓がコレステロールを下げるための標的器官であることを示しています。生体内および生体外の試験により、ロスバスタチンは細胞表面の肝LDL受容体の数を増加させ、それによりLDLの取り込みと異化を促進し、肝臓VLDL合成を阻害し、それによりVLDLおよびLDL粒子の総数を減らすことが示されました
ホモ接合およびヘテロ接合の家族性高コレステロール血症患者、非家族性高コレステロール血症患者、混合型脂質異常症患者の場合、ロスバスタチンは総コレステロール、LDL-C、ApoB、非HDL-Cレベルを低下させることができます。また、ロスバスタチンはTGを低下させ、HDL-Cレベルを上昇させます。高トリグリセリド血症のみの患者では、ロスバスタチンは総コレステロール、LDL-C、VLDL-C、ApoB、非HDL-C、TGレベル、およびHDL-Cレベルの上昇を減少させました。ロスバスタチンが心血管系の罹患率と死亡率に及ぼす影響は明らかにされていません。
毒性研究
中枢神経系毒性
いくつかの類似の薬物のイヌ試験で、CNS血管損傷が観察され、血管周囲出血、浮腫、および血管周囲単核細胞浸潤が観察されました。このクラスの薬物と構造が類似した薬物は、犬の人間の最大推奨用量の平均濃度の30倍の用量で、用量依存性の視神経変性(網膜膝体線維ウォーラー変性)を示します。
1匹のメス犬にロスバスタチン90 mg / kg /日を経口投与し(AUCに従って計算、全身暴露はヒト40 mg /日暴露の100倍に相当)、24日目に突然死して安静になり脈絡叢を示した浮腫、出血、部分的な壊死。イヌにロスバスタチン6 mg / kg /日を経口投与し(AUCに従って計算、全身暴露はヒト40 mg /日暴露の20倍に相当)、角膜は52週間濁っていた。ロスバスタチン30 mg / kg /日のイヌ経口投与(AUCによると、全身曝露はヒト40 mg /日曝露の60倍に相当します)、12週間、白内障が見られます。ロスバスタチン90 mg / kg /日のイヌ経口投与(AUCによると、全身曝露はヒト40 mg /日曝露の100倍に相当します)、4週間、目に見える網膜形成異常と網膜剥離。イヌは30 mg / kg /日以下の用量で1年間連続して投与され(AUCにより計算され、ヒト40 mg /日への60回の曝露に相当する全身曝露)、網膜への影響は観察されなかった。
遺伝毒性
エメス試験、マウスリンパ腫試験、CHL細胞染色体異常試験、およびマウス小核試験におけるロスバスタチンの結果はすべて陰性でした。
生殖毒性
ラットの生殖能力試験では、オスのラットに、交配前の9週目から5、15、50 mg / kg /日、メスのラットの交配の2週間前に、最高用量(AUCによる)で経口投与しました。全身暴露は、ヒトの40 mg /日暴露の10倍に相当すると推定されており、生殖能力への悪影響はありません。犬にロスバスタチン30 mg / kg /日を1か月間経口投与し、精巣で精原細胞(精子様巨大細胞)を観察しました。サルにロスバスタチン30 mg / kg /日を6か月間投与し、マクロファージおよび輸精管に空胞を形成しました。上記のイヌとサルの用量は、それぞれ40 mg /日の体表面積の20倍と10倍と推定されました。同様の現象は、同様の薬物でも見られます。
雌ラットに、交配7日後に5、15、50 mg / kg /日、高用量群(AUCとして計算、全身暴露はヒト40 mg /日暴露の10倍に相当)を経口投与しました。骨化遅延。
ラットには、妊娠7日目から授乳21日目(離乳)に2、10、50 mg / kg /日、および高用量群(体表面積、ヒト40mg /日の12倍以上で計算)を経口投与しました。子供の生存率は低下します。妊娠6日目から授乳18日目(離乳)まで0.3、1、3 mg / kg /日をウサギに経口投与(体表面積で計算、40 mg /日に相当)、胎児の生存率の低下、母動物死。ロスバスタチンの投与量は、ラットで≤25mg / kg / day、ウサギで≤3mg / kg / dayであり、催奇形性は認められなかった(それぞれ40 mg / dayのヒト暴露に匹敵するAUCおよび体表面積として計算)。
発がん性
ラットの104週間発がん性試験では、経口投与量は2、20、60、80 mg / kg /日でした。 80mg / kg /日(AUCで計算、全身暴露はヒト40mg /日暴露の20倍に相当)。子宮ポリープの発生率は用量群の女性群で有意に増加し、低用量では発生率は増加しなかった。
マウスの107週間発がん性試験では、経口投与量は10、60、200 mg / kg /日でした。 200mg / kg /日(AUCにより計算、全身暴露はヒト40mg /日暴露の20倍に相当)。用量群は肝細胞腺腫/発癌の増加を示し、低用量の増加はなかった。
[薬物動態]
白人のロスバスタチンの薬物動態学的研究は以下を示した:
吸収:血中濃度は、経口投与の5時間後にピークに達しました。絶対バイオアベイラビリティは20%です。
分布:ロスバスタチンは、コレステロール合成およびLDL-Cクリアランスの主要な部位である肝臓によって大量に摂取されます。ロスバスタチンの流通量は約134Lです。ロスバスタチンの血漿タンパク質結合率(主にアルブミン)は約90%です。
代謝:ロスバスタチンの限られた代謝(約10%)。ヒト肝細胞を用いたin vitro代謝研究により、ロスバスタチンはシトクロムP450代謝の弱い基質であることが示されています。代謝に関与する主要なアイソザイムは、CYP、2C9、2C19、3A4、および2D6であり、これらは代謝にあまり関与していません。既知の代謝物は、N-デメチルおよびラクトン代謝物です。 N-デメチル代謝物の活性はロスバスタチンの活性よりも50%低いが、ラクトン代謝物は臨床的に不活性であると考えられている。
循環HMG-CoAレダクターゼに対する阻害活性の90%以上がロスバスタチン由来です。
排泄:ロスバスタチンの投与量の約90%は、元の形で排泄物(吸収された活性物質と吸収されていない活性物質を含む)で排泄され、残りは尿中に排泄されます。尿の約5%が元の形状です。血漿排出半減期は約19時間です。排出半減期は、用量を増やしても増加しません。血漿クリアランスの幾何平均は約50 L / hr(変動係数21.7%)でした。他のHMG-CoAレダクターゼ阻害剤と同様に、肝臓によるロスバスタチンの取り込みには、膜輸送体OATP-Cが関与します。このトランスポーターは、ロスバスタチンの肝クリアランスに重要です。
直線性:ロスバスタチンへの全身暴露は、用量に比例して増加しました。複数回投与後の薬物動態パラメーターは変化しませんでした。
ロスバスタチンの経口投与の約10%のみが代謝され、主にN-脱メチル化が行われます。
特別な人口:
年齢と性別:年齢または性別は、ロスバスタチンの薬物動態に臨床的に有意な影響を与えません。
腎不全:腎機能障害の程度が異なる患者を対象とした海外での研究では、軽度および中等度の腎疾患は、ロスバスタチンまたはN-デスメチル代謝物の血漿濃度に影響を与えませんでした。ただし、健康なボランティアと比較して、重度の腎障害(クレアチニンクリアランス<30 ml / min)の患者では、血漿濃度が3倍増加し、N-デスメチル代謝物の血漿濃度が9倍増加しました。血液透析患者のロスバスタチンの定常状態血漿濃度は、健康なボランティアの血漿濃度よりも約50%高くなっています。
肝不全:外国の肝機能障害の程度が異なる患者の研究では、Child-Pughスコアが7以下の被験者が曝露を増加させたという証拠はありませんでしたが、2症例では8のChild-Pughスコアがありました-9の患者では、ロスバスタチンへの曝露は、Child-Pughスコアが低い患者よりも少なくとも2倍高かった。 Child-Pughスコアが9を超える被験者の経験はありません。
民族性:外国の薬物動態学的研究は、アジア人(中国人を含む)被験者の血漿濃度-時間曲線(AUC)の下の領域の中央値とピーク濃度(Cmax)が西部白人のものであることを示しています。 2回。集団の薬物動態分析により示された。白人グループと黒人グループの間で、薬物動態に臨床的に関連する違いはありませんでした。
研究では、中国人健康志願者の単回投与後、tmaxの中央値は2.5〜5時間であり、その後指数関数的に減少することが示されています。半減期(t1 / 2)は約11〜12時間です。複数回投与の3日目に、血漿濃度は定常状態に達した。複数回投与後の薬物蓄積はわずかです。そして、用量に関係なく。
[保管]遮光、密閉、涼しい場所(20°C以下)で保管。
[梱包]ダブルアルミ包装、7個/箱、14個/箱、21個/箱、28個/箱。
[有効期間] 24か月
[実行基準]国立食品医薬品局標準YBH04172008
[承認番号]
(1)5mg:漢方薬H20080240;
(2)10mg:National Drug Standard H20080241;
(3)20mg:National Drug Standard H20080242。
[メーカー]
会社名:Lunan Beite Pharmaceutical Co.、Ltd.
生産住所:山東省臨y市銀que山路243号
郵便番号:276006
電話番号:0539-8336336(販売)8336337(品質管理部)
FAX番号:0539-8336029(販売)8336338(品質管理部)
ウェブサイト:www.LUNAN.com.cn
24時間対応のカスタマーサービスホットライン:400-0539-310